0
Porównywać
0
Porównywać
 0
Kosz
0
Kosz

Chromatografia
Kolumny ChromShell i rozpuszczalniki
Stosując kolumny HPLC ChromShell®, należy wziąć pod uwagę kilka ważnych cech rozpuszczalników organicznych stosowanych w fazie ruchomej. Lepkość jest najważniejszym parametrem, ponieważ rozpuszczalniki o wysokiej lepkości są przyczyną wzrostu przeciwciśnienia w układzie HPLC. Inne ważne parametry to " Odcięcie UV ", wskaźnik polarności i cena. Rozpuszczalniki o wysokiej wartości granicznej parametru „UV” pogorszyć czułość w detektor UV / VIS i niskiej polarności rozpuszczalnika spowodowania szybkiego wydzielania związków organicznych, i są powszechnie stosowane do czyszczenia lub regeneracji kolumny.
Acetonitryl
jest prawdopodobnie najlepszym rozpuszczalnikiem organicznym stosowanym w mieszaninie z wodą, ponieważ zapewnia najniższe ciśnienie wsteczne w systemach HPLC. Jednocześnie ma bardzo niskie " odcięcie UV ", a tym samym doskonałą czułość w detektorach UV / Vis. Największym minusem jest jego cena, która ostatnio znacznie wzrosła.
Metanol
jest innym bardzo popularnym rozpuszczalnikiem mającym podobną siłę wymywania jak acetonitryl, ma stosunkowo niską absorbancję UV i jest znacznie tańszy niż acetonitryl. Główną wadą metanolu, gdy jest stosowany z kolumnami HPLC o niskim rozmiarze cząstek jest tworzenie się wyższego ciśnienia wstecznego, które może przekraczać granicę HPLC przyrządu.
Aceton
to mniej zużyty rozpuszczalnik ze względu na wysoką absorpcję promieniowania UV. Czasami stosuje się go w analizach związków absorbujących przy wyższych długościach fal lub w połączeniu z innymi typami detektorów, np. MS.
Etanol
zwykle nie jest zalecany do stosowania z HPLC. Mieszanie z wodą powoduje wysokie ciśnienie wsteczne.
Iso-, n-propanol
mają stosunkowo silną siłę wymywania i są używane głównie do czyszczenia kolumn przy niskich przepływach, ponieważ generują one również wysokie przeciwciśnienie.
Tetrahydrofuran
ma podobną moc wymywania, jak n-propanol, ale ze względu na wyższą cenę jest stosowany rzadziej.
Dezaktywacja szkła
Dezaktywuj szkło za pomocą DMDCS
Dimetylodichlorosilan (DMDCS) reaguje z aktywnymi grupami hydroksylowymi obecnymi na powierzchni szkła, tworząc dezaktywowaną powierzchnię. Proces ten jest wykonywany przez obojętne szklane naczynia przeznaczone przede wszystkim dla wrażliwych związków.
Procedura
Podczas dezaktywacji powstaje chlorowodór (HCl). Dlatego konieczne jest wyłączenie maski.
- Użyj 5% DMDCS w toluenie, aby dezaktywować. Roztwór można wytworzyć przez rozpuszczenie 20 ml DMDCS w 400 ml toluenu. Przechowywać roztwór w ciemnym szklanym pojemniku w temperaturze pokojowej.
- Zanurzyć szklane pojemniki do dezaktywacji w 5% DMDCS przez 15 do 30 minut.
- Opłucz szkło dwukrotnie toluenem.
- Zanurz szkło w metanolu na 15 minut.
- opłucz szklankę metanolem.
- Wysuszyć szkło czystym azotem (bez wilgoci i węglowodorów).
Ustawienie prędkości liniowej
Prędkość liniowa jest ważnym parametrem w chromatografii, co ma wielki wpływ na skuteczność oddzielania. Dlatego ważne jest opracowanie metod deadweight i określenia czasu.
Liniowy pomiar prędkości w GC
Czas martwy określa się przez natryskiwanie 2 μl związku, który nie ma retencji w kolumnie chromatograficznej i jest wykrywalny przez zastosowany detektor. Używając strzykawki gazoszczelnej, weź fazę gazową lub gazową związku i dozuj na chromatograf. Dokładnie zmierzyć czas wtrysku i czas wymywania, z którego określa się czas martwy.
| Detektor | Związek |
|---|---|
| FID | metan, propan, butan |
| ECD | chlor, powietrze (przy niskiej temperaturze termostatu) |
| TCD | metan, butan, powietrze (przy niskiej temperaturze termostatu) |
| NPD | acetonitryl, powietrze (przy niskiej temperaturze termostatu) |
| MS | propan, butan, argon, powietrze (przy niskiej temperaturze termostatu) |
| PID | acetylen, etylen |
Uwaga: Niektóre związki mogą mieć niewielką retencję na kolumnach grubowarstwowych, ale mogą być odtwarzalne dla podobnych typów kolumn.
Zastosowanie chiralnych kolumn
Czy wiesz, jak poprawnie używać chiralnych kolumn celulozowych/amylozowych?
Kolumny chiralne są transportowane w n-heksanie/2-propanolu (9: 1, v/v). Każda kolumna jest indywidualnie testowana i zawsze zaopatrzona w certyfikat jakości i parametry separacji do oznaczania tlenku trans-stylibenu .
Korzystanie z faz mobilnych
Kolumny Lux można stosować zarówno w fazie normalnej (mieszaniny n-alkanów / alkoholi) w fazie odwróconej (woda / MeOH, woda / ACN i bufor / MeOH i bufor/ACN) lub polarne rozpuszczalniki organiczne (100% ACN, niższe alkohole i ich mieszaniny).
Zgodność faz mobilnych
Zmieniając fazę ruchomą, zawsze należy postępować zgodnie z zalecaną procedurą mycia kolumn. Konieczna jest ocena mieszalności rozpuszczalników stosowanych każdorazowo. W celu bezpiecznego przekształcenia kolumny z heksanu w metanol (ACN) i odwrotnie, zawsze stosować jako rozpuszczalnik transportowy 100% 2-propanol przy przepływie 0,2 - 0,5 ml/min. Aby niezawodnie usunąć oryginalną fazę ruchomą, przepłukać kolumnę około 10 razy większą niż objętość kolumny (tj. 25 ml 100% 2-propanolu dla kolumny 250 x 4,6 mm, 15 ml dla 150 x 4,6 mm). Dodatkowo, jeśli bufor nie miesza się z 2-propanolem, przepłukać kolumnę przed i po użyciu tego buforu z 100% wody.
Używanie modyfikatorów fazy ruchomej
W przypadku niektórych kwaśnych lub zasadowych środków chiralnych, do uzyskania odpowiedniej separacji chiralnej lub pożądanego kształtu piku, należy zastosować specyficzne modyfikatory MF. W próbkach zasadowych można stosować dietyloaminę, etanoloaminę lub butyloaminę w stężeniach 0,1 - 0,5 %, natomiast kwas octowy lub kwas trifluorooctowy zazwyczaj w stężeniu 0,1 - 0,2 % w przypadku próbek kwaśnych. Możliwe są również mieszaniny dodatków zasadowych i kwasowych, np. Octan dietyloaminy lub trifluorooctan. Kolumny Lux dają te same wyniki, stosując wszystkie wyżej wymienione rozpuszczalniki i modyfikatory MF we wskazanych stężeniach.
Niezgodne rozpuszczalniki
Kolumny chiralne są wytwarzane przez wiązanie różnych pochodnych polisacharydów z powierzchnią żelu krzemionkowego. Dlatego wszystkie rozpuszczalne w rozpuszczalnikach pochodne polisacharydów nie mogą stykać się z fazą stacjonarną, nawet przy dowolnym stężeniu, np. THF, aceton, chlorowane węglowodory, octan etylu, dimetylosulfotlenek, DMF, N-metyloformamid i tym podobne.
Limit ciśnienia
Przepływ fazy ruchomej należy tak ustawić, aby ciśnienie wsteczne nie przekraczało 300 barów (4300 psi).
Temperatura pracy
Stosując standardowe fazy ruchome (takie jak n-alkan / alkohole), zakres temperatur kolumn Lux wynosi 0-50 ° C.
Przechowywanie kolumn
Przy dłuższym przechowywaniu zaleca się przechowywanie kolumn w n-heksanie/2-propanolu (9: 1, v/v). Kolumny użyte w odwróconym MF należy najpierw przemyć wodą (gdy bufor był stosowany jako modyfikator MF), a następnie samym metanolem i / lub metanolem, jeśli bufor nie był używany. Kolumnę można również przechowywać w metanolu.
Przedłużyć żywotność kolumn
Chromservis zaleca stosowanie systemu kolumn zabezpieczających uchwyt kolumny przedniej i odpowiednich kolumn wstępnych, aby zapewnić długotrwałą i bezproblemową separację kolumn, szczególnie w przypadku rozdzielania próbek uzyskanych ze złożonych i złożonych macierzy. Optymalnie, próbka powinna zostać całkowicie rozpuszczona w odpowiednim MF, a następnie przefiltrowana przez filtr strzykawkowy o porowatości 0,45 μm.
Wskazówki i porady
 Ta strona zawiera informacje techniczne, wskazówki i porady dotyczące podejmowania decyzji i zaleceń dotyczących wyboru akcesoriów chromatograficznych.
Ta strona zawiera informacje techniczne, wskazówki i porady dotyczące podejmowania decyzji i zaleceń dotyczących wyboru akcesoriów chromatograficznych.
- Dynamiczna przestrzeń headspace
- Instalacja kolumn GC
- Jak radzić sobie z chiralnymi kolumnami HPLC
- Linery dla GC
- Optymalne ustawienie prędkości liniowej
- Instrukcje dotyczące dezaktywacji naczyń szklanych
- Procedura kondycjonowania kolumn GC
- Desorpcja termiczna
- Konserwacja strzykawek
- Wybór septa GC
- Wybór kolumn LC
- Wybór końcówki strzykawki
- Zwiększona szczelność wtryskiwaczy GC Agilent
- Poprawianie szczelności połączeńKolumny kapilarne GC
- Zwiększony stosunek sygnału do szumu w systemach GC
- Zwiększona wydajność separacji LC
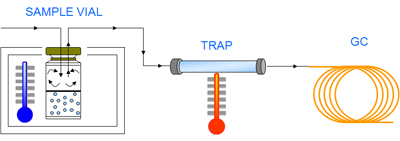
Dynamiczna przestrzeń headspace
Metoda Dynamic Headspace (DHS) jest stosowana w szerokim zakresie aplikacji środowiskowych. Największe zastosowanie ma w analizie lotnych związków organicznych (LZO) w piciu, metodzie, powierzchni i ściekach. Te matryce zawierają mieszaninę związków o różnej polarności i lotności (chlorowane węglowodory, aromatyczne węglowodory, związki tlenu i podobne). Dynamiczna przestrzeń nad powierzchnią jest również używana dla tych aplikacji:
- charakterystyka przypraw, ziół, żywności, mydeł i substancji zapachowych
- oznaczanie resztkowych monomerów i LZO w polimerach
- analiza pozostałości rozpuszczalników w opakowaniach żywności i produktach farmaceutycznych
- weryfikacja "żywności ekologicznej"
- analiza śladowa aktywnych składników farmaceutycznych
- analiza metabolitów w płynach biologicznych (węglowodory aromatyczne w moczu, benzen we krwi)
Instalacja kapilarnych kolumn GC
 Krótka procedura instalowania kapilarnych kolumn GC
Krótka procedura instalowania kapilarnych kolumn GC
- Ochłodzić wszystkie ogrzewane strefy GC
- Sprawdź środki do czyszczenia gazu i wymień w razie potrzeby
- oczyścić wtryskiwacz i detektor
- Wymień wkładkę wtryskiwacza / detektora na nową
- Wymień ważne uszczelki w inżektorze i detektorze
- Wymień przegrodę we wtryskiwaczu
- Ustaw przepływ gazów detektora
- Dokładnie sprawdź kolumnę, jeśli nie jest uszkodzona
- Przymocuj nakrętkę i skuwkę do każdego końca kolumny
- Cięcie 10 centymetrów z każdego końca kolumny. Do wycinania kolumn kwarcowych użyj szafirowego noża lub płyty ceramicznej. Do wycinania metalowych kolumn użyj płytki ceramicznej lub kwadratowego pilnika. Narzędzia do cięcia kolumn można znaleźć w naszym katalogu.
- Zawieś kolumnę kapilarną na uchwytach termostatu GC, aby uniknąć uszkodzenia
- Włóż żądany koniec kolumny do wtryskiwacza. Aby uzyskać prawidłową długość, należy zapoznać się z instrukcją obsługi GC.
- Zamontuj kolumnę tak, aby nie dotykała ścianek termostatu
- Ustaw natężenie przepływu według kolumny zgodnie z parametrami podanymi na chromatogramie testowym producenta
- Ustaw współczynnik podziału, płukanie przegrody i inne parametry zgodnie z wymaganiami producenta GC
- Upewnić się, że gaz nośny przepływa przez kolumnę. Zanurz wolny koniec kolumny w fiolce z rozpuszczalnikiem (aceton lub izopropanol).
- Włóż pożądany koniec kolumny do wykrywacza. Aby uzyskać prawidłową długość, należy zapoznać się z instrukcją obsługi GC.
- Sprawdzić szczelność kolumny za pomocą czujnika przewodnictwa cieplnego. Nie należy używać wody z mydłem ani wykrywaczy nieszczelności, ponieważ kolumna może ulec uszkodzeniu.
- Ustaw temperaturę wtryskiwacza i czujkę. Włącz wykrywacz po stabilizacji. Uwaga - Należy uważać, aby nie przekroczyć maksymalnej dozwolonej temperatury kolumny!
- Teraz ustaw prawidłową objętość martwą (prędkość liniową), rozpylając metan lub inny związeknie jest zatrzymywany przez kolumnę.
- Sprawdź kształt piku, który powinien być symetryczny
- Koncentrować kolumnę w maksymalnej temperaturze do momentu ustabilizowania linii bazowej detektora (maksymalna temperatura zastosowana w kolumnie z chromatogramem).
- Ustaw temperaturę termostatu i ponownie wstrzyknij metan lub inny, związek nie zatrzymany przez kolumnę. Dostosuj warunki dla optymalnej prędkości liniowej.
- Wstrzyknąć zduplikowaną mieszaninę testową kolumny i sprawdzić stan kolumny i całego układu chromatograficznego
- Skalibruj instrument, a teraz możesz pobierać próbki
Uwaga: Jeśli nowa kolumna, należy wykonać klimatyzację przed ustawieniem optymalnego czasu martwego.
Konwersje jednostek
Kapilarna objętość HPLC
| ID (mm) | ID (cal) | μl / cm | μl / cal | ID (mm) | ID (cal) | μl / cm | μl / cal | |
|---|---|---|---|---|---|---|---|---|
| 0,050 | 0,002 " | 0,02 | 0,05 | 1,00 | 0,040 " | 7,85 | 20,59 | |
| 0,064 | 0,0025 " | 0,03 | 0,08 | 1,40 | 0,055 " | 15.39 | 38,93 | |
| 0,075 | 0,003 " | 0,04 | 0.12 | 1.52 | 0,060 " | 18.15 | 46,33 | |
| 0.10 | 0,004 " | 0,08 | 0,21 | 1.59 | 0,062 " | 19,86 | 49,47 | |
| 0.13 | 0,005 " | 0.13 | 0,32 | 1,65 | 0,065 " | 21,38 | 54,38 | |
| 0.17 | 0,0067 " | 0,23 | 0,58 | 1.70 | 0,067 " | 22,70 | 57,78 | |
| 0,18 | 0,007 " | 0,25 | 0,63 | 1,78 | 0,070 " | 24,88 | 63.06 | |
| 0,25 | 0,010 " | 0,49 | 1.29 | 2,00 | 0,079 " | 31,42 | 80,32 | |
| 0,38 | 0,015 " | 1.13 | 2,90 | 2.10 | 0,083 " | 34,64 | 88,66 | |
| 0,50 | 0,020 " | 1,96 | 5.15 | 2.16 | 0,085 " | 36,64 | 92,99 | |
| 0,75 | 0,030 " | 4,42 | 11,58 | 2,40 | 0,094 " | 45,24 | 113,72 |
Dodatek UV odcinający fazę ruchomą
| Przyłączeniowy | Odcięcie UV (nm) |
| Kwas octowy, 1% | 230 |
| Octan amonu, 10 mM | 205 |
| Węglan amonu, 10 mM | 190 |
| Wodorofosforan amonu, 50 mM | 205 |
| CAPS kwas 3-(cykloheksyloamino)etanosulfonowy, 0,1% | 215 |
| EDTA, 1 mM | 190 |
| Kwas solny, 0,1% | 190 |
| Wodorofosforan wapnia, 10 mM | 190 |
| Wodorofosforan wapnia, 10 mM | 190 |
| MES Kwas 2-(N-morfolino)etanosulfonowy, pH 6,0, 10 mM | 215 |
| Octan sodu, 10 mM | 205 |
| cytrynian sodu, 10 mM | 225 |
| Dodecylosiarczan sodu, 10 mM | 190 |
| Mrówczan sodu, 10 mM | 200 |
| Kwas heksanosulfonowy sodu, 5 mM | 225 |
| TEA, (trietyloamina), 1% | 235 |
| TFA (kwas trifluorooctowy), 0,1% | 190 |
| Diwodorofosforan tetrabutyloamoniowy, 5 mM | 200 |
| TRIS HCl (Tris(hydroksymetylo)aminometan), pH 7,0, 20 mM | 202 |
| TRIS HCl (Tris(hydroksymetylo)aminometan), pH 8,0, 20 mM | 212 |
Konwersja jednostek i tabel
 Konwersje jednostek on-line:
Konwersje jednostek on-line:
- Przydatne wykresy w chromatografii i jednostkach online
- Kwasy i zasady pK stosowane jako dodatek do HPLC w fazie ruchomej
- Dodatek odcięcia UV dla fazy ruchomej
- Dobór kolumny w zależności od wielkości oprysku i jego pojemności
- Wybór kapilar dla różnych przepływów
- Oszacowanie ciśnienia na kolumnach, w zależności od wielkości cząstek, średnicy i długości kolumny
- Zależność lepkości mieszaniny rozpuszczalników od jej składu procentowego
- Właściwości rozpuszczalnika
- Konwersja jednostek wielkości cząstek
- Konwersja metody z porowatej cząstki na ChromShell (PRZYGOTOWUJEMY)